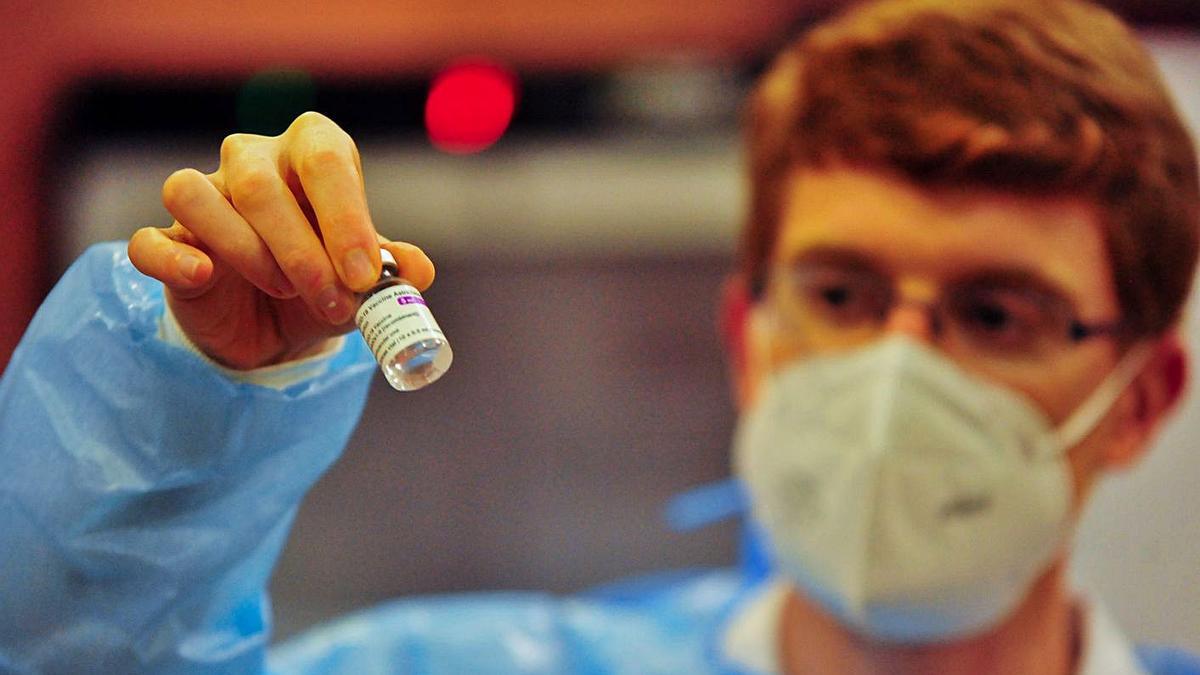
El Ministerio de Sanidad acordó ayer inmunizar con la vacuna de AstraZeneca solo a la población mayor de 60 años. La propuesta la planteó Carolina Darias en el Consejo Interterritorial del Sistema Nacional de Salud (CISNS) celebrado ayer por la tarde-noche, después de la reunión extraordinaria de los ministros europeos de Sanidad para analizar el informe de la Agencia Europa del Medicamento (EMA) sobre los efectos secundarios de la vacuna de AstraZeneca.
La decisión no afecta a los 55.000 gallegos llamados a vacunarse estos días con los viales de Oxford porque todos tienen 60 años o más, pero hasta ahora en Galicia y en el resto del país se utilizaban los viales de la polémica vacuna para inmunizar a profesionales esenciales como sanitarios, trabajadores de residencias, profesores, policías, ... sin límite de edad. La comunidad gallega ha recibido 180.000 dosis de esta fórmula.
El Gobierno de España toma esta decisión después de que la EMA reconociese que existe “un posible vínculo” entre las personas vacunadas con el antídoto de AstraZeneca, particularmente mujeres de menos de 60 años, y los casos muy raros de coágulos sanguíneos inusuales notificados. Eso sí, la EMA insiste en que los beneficios generales de utilizar esta vacuna en la prevención del COVID-19 siguen superando ampliamente los riesgos de los posibles efectos secundarios.
Por ello, la EMA no recomienda por el momento limitar o restringir el uso de la vacuna e insiste en que debe seguir utilizándose porque el virus sigue provocando miles de muertes cada día. Sin embargo, España por “un principio de precaución” ha restringido su utilización.
“El riesgo de mortalidad del COVID-19 es muy superior al riesgo de los efectos secundarios”, explicaba ayer la directora ejecutiva de la EMA, Emer Cooke, que también recordó que la vacuna ha demostrado ser muy eficaz a la hora de evitar los casos graves de la enfermedad y la hospitalización.
Rechazo de Madrid
La Comunidad de Madrid ya rechazó ayer la propuesta de Sanidad de parar temporalmente la vacunación con AstraZeneca en menores de 60 años porque, en su opinión, no está basada en las conclusiones de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés).
“El comité de seguridad de la EMA ha concluido que los coágulos de sangre inusuales con plaquetas bajas en sangre deben incluirse como efectos secundarios muy raros de Vaxzevria (como se denomina ahora a la vacuna de AstraZeneca)”, confirmó ayer la Agencia Europea del Medicamento tras una nueva revisión realizada por el comité de farmacovigilancia (PRAC) que sostiene que una explicación plausible para la combinación de coágulos sanguíneos y plaquetas bajas en sangre “es una respuesta inmune que conduce a una condición similar a la que se observa a veces en pacientes tratados con heparina”.
Por ello, la EMA ha vuelto a recomendar a los profesionales sanitarios y a todas las personas que reciban la vacuna de AstraZeneca, recomendada para todos los adultos de más de 18 años, que sean conscientes de la posibilidad de trombos durante las dos semanas posteriores a recibir la inyección. Hasta ahora, según explicó la directora ejecutiva, Emer Cooke, la mayoría de los casos se han producido en mujeres de menos de 60 años aunque con las evidencias actualmente disponibles “no se han confirmado factores de riesgo específicos”, ni debido al género, la edad o condiciones médicas previas.
“Aunque la mayoría de los casos han ocurrido en personas de menos de 60 años y en mujeres, por las diferentes formas en que se utiliza la vacuna en diferentes países, el PRAC no ha llegado a la conclusión de que la edad y el sexo sean factores de riesgo claros para estos efectos secundarios tan raros”, explicó su responsable, Sabine Strauss, que explicó que es el motivo por el que no recomiendan ninguna medida específica para reducir el riesgo.
Casos de trombosis
La publicación del nuevo análisis se aceleró por las declaraciones del responsable de la estrategia de vacunas de la agencia, Marco Cavaleri, al diario italiano ‘Il Messaggero’ este pasado martes en las que avanzaba la existencia de un vínculo entre los casos de trombosis y la vacuna de la farmacéutica anglosueca.
El comité de seguridad y farmacovigilancia (PRAC) de la agencia ha analizado en las últimas semanas 62 casos de trombosis venosa cerebral (CVST) y 24 de trombosis esplénica venosa notificados hasta el 22 de marzo, y de los cuáles 18 fueron fatales, aunque hasta el 4 de abril los casos notificados al sistema EudraVigilancia suman 169 y 53 respectivamente en una población de 34 millones de personas vacunadas en el Espacio Económico Europeo y el Reino Unido.
Países como Dinamarca o Noruega tras las dudas iniciales ya suspendieron la administración de esta vacuna. Otros países como Suecia, Finlandia o Alemania ya la usan solo para mayores de 60 años.